Основные достижения 2016 г.
Электрокалорический эффект в триглицинсульфате в неравновесных термодинамических условиях
Впервые экспериментально реализован метод охлаждения на основе электрокалорического эффекта в периодическом электрическом поле в неравновесных тепловых условиях. Наиболее привлекательным аспектом является гипотетическая возможность реализации системы охлаждения, не требующей тепловых ключей (рис.1).
При стабилизации температуры основания образца Tbot, периодическое электрическое поле вдоль сегнетоэлектрической оси b вызывает появление градиента температуры и теплового потока от «свободного» торца к термостатированному основанию.
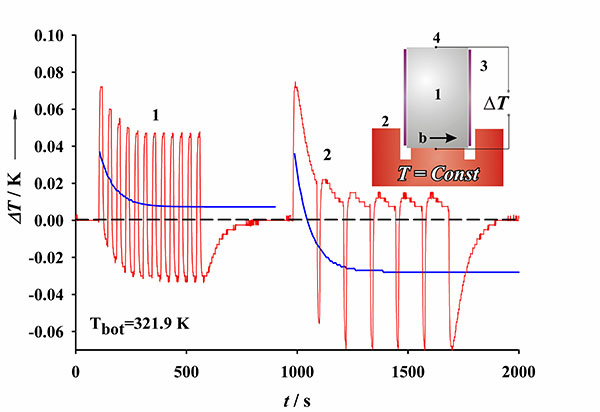
Рис. 1. Схема электрокалорического элемента и зависимости от времени ΔT = Тtop - Tbot в поле Е = 3 kV∙cm-1 при f = 0.025 Hz (1) и f = 0.008Hz (2). Сплошные линии соответствуют средней разности Тtop - Tbot.
Bondarev V.S., Mikhaleva E.A., Gorev M.V., Flerov I.N. Intensive electrocaloric effect in triglycine sulfate under nonequilibrium thermal conditions and periodic electric field // Physica Status Solidi B - 2016. - v. 253, issue 10, p. 2073-2078.
Разработка биомагнитных наноустройств и приборов ранней диагностики и управляемой электромагнитными полями таргетной терапии
В результате комплексных междисциплинарных исследований, совместно с ИХХТ и КрасГМУ, созданы технологии получения биомагнитных наноустройств, состоящих из металлических наночастиц иммобилизированных фрагментами одноцепочечных ДНК (аптамерами). Физические свойства наночастиц обеспечивают функциональность данных биомагнитных наноустройств для управляемой электромагнитными полями таргетной терапии (лазерная гипертермия и механическое разрушение раковых клеток в низкочастотном магнитном поле), а использование ДНК- аптамеров обеспечивает адресность воздействия на раковые клетки.

Рис. 2. А) Наноконьюгаты наночастиц никеля с осажденными на их поверхности наночастицами золота.
В) Мышка после введения ей бионаноконьюгатов, помещенная в переменное магнитное поле.
С) разрушенные раковые клетки
D) ПЭТ-КТ мыши с использованием метки радиоактивной глюкозы, после сеансов лазерной гипертермии с введением наночастиц золота иммобилизованных ДНК -аптамерами.
Разработаны методики и опытный образец аппаратно программного комплекса, на основе дихрометра кругового дихроизма СКД-2МУФ, позволяющие фиксировать следовые количества продуктов жизнедеятельности раковых клеток в биологических жидкостях, а также осуществлять управляемую электромагнитными полями таргетную терапию раковых клеток (рис.2).
- Zamay Tatiana N., Sokolov Alexey E., Shabanov Alexandr V. et.al // Nucleic Acid Therapeutics. December 2016, ahead of print. doi:10.1089/nat.2016.0634.
- Galina S. Zamay, Tatiana N. Zamay, Alexey E. Sokolov et.al //Scientific Reports 6, Article number: 34350 (2016) doi:10.1038/srep34350
- P.D. Kim, S.S. Zamay, A.E. Sokolov, et.al// Doklady Biochemistry and Biophysics, 2016, Vol. 466, pp. 66–69.
Операции с документом
